愛滋病被喻為二十世紀黑死病;許多癌症到現在還是神仙難治!隨著生物醫學研究日新月異,這些令人聞之色變的惡疾,透過滴血檢測就會被逼出原形,揪出元凶的神兵利器全是利用蛋白質抗原抗體的專一性結合打造而成。
蛋白質的檢驗方法
蛋白質是維持生命正常運作的重要分子,也是遺傳物質表現的最終產物,許多疾病的發生往往跟蛋白質的質或量改變有關。不僅僅是人體,細菌或病毒也是由蛋白質組成,成為科學家揪出疾病的關鍵角色!
傳統的蛋白質檢測方式包含酵素免疫分析法 (Enzyme-linked immunosorbent assay,ELISA) 與西方墨點法 (Western blot),都是利用抗原抗體結合特性進行檢驗。雖可透過定性或定量檢測蛋白質的表現,卻是耗時費工,需由專業人員在實驗室操作設備分析,這也是病患到醫院抽血,總是要等到下次回診才能檢驗看報告的原因。
然而等待結果出爐的時間卻讓人如坐針氈,所幸目前已有許多疾病可以透過快篩試劑,簡易而快速的知道檢驗結果。蛋白質晶片就是醫師快速診斷的好幫手,尤其是面對傳染病爆發大流行,例如流感病毒或新冠肺炎,透過快篩除了能夠及時隔離阻絕疫情蔓延,更可以及早診斷及早治療,降低重症死亡率。但蛋白質晶片如此便利,還是有發展瓶頸亟待突破。
蛋白質晶片的困境
蛋白質晶片雖快速便利,但靈敏度比不上傳統檢驗方式,成為最大缺點。此外,製作上亦有許多困難必須克服。首先,蛋白質分子是立體結構,容易受到環境影響而變化,甚至失去活性,且每種蛋白質維持穩定的條件又不盡相同。再者,蛋白質抗原抗體的結合具專一性,也就是說兩者僅在特定位置結合,每個抗體在晶片生產過程被固定的方向都不一樣,就像被颱風掃過的森林公園,歪七扭八不規則排列,導致許多抗體無法有效跟抗原結合,大幅降低晶片檢測效能。
神奇的EOP技術
如何使抗體乖乖聽話整齊站好,提高檢驗效能,成為蛋白質晶片發展的重要議題,財團法人國家實驗研究院臺灣半導體研究中心研究員陳惠民帶領團隊,成功開發蛋白質效能最大化 (Efficiency optimization of protein on chip,簡稱EOP) 技術,有效解決抗體在晶片上面東倒西歪的亂象,就像是無形的魔手把抗體排列整齊地種在晶片上!
蛋白質本身帶有著不同的電性,抗體蛋白也不例外。研究團隊利用蛋白質帶電特性在晶片外加一個電場,透過正負極的電場互相牽引的原理,當電場方位改變,抗體就會跟著調整角度,讓所有帶電抗體朝相同方向整齊排列。在蛋白質晶片製造過程,透過調整電場與晶片的角度,控制抗體的方向,並找出抗原抗體的最佳結合角度,提升蛋白質晶片檢測效能。
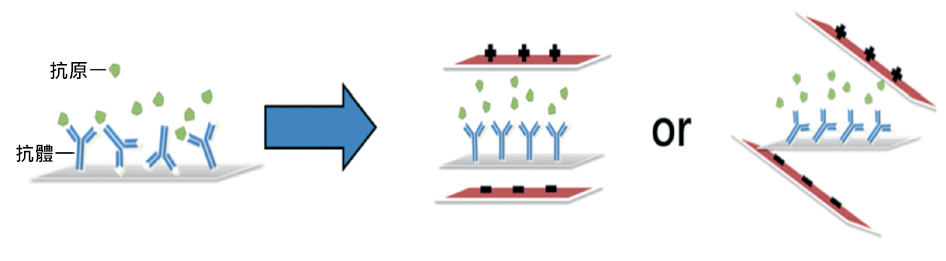
圖一:EOP技術示意圖:(箭頭左側)未在晶片外加電場,抗體方向沒有一致性。(箭頭右側)晶片外加電場以後,抗體方向呈現一致性,並透過改變電場方位調整抗體排列角度。圖/Wu et al., 2015。
EOP技術的應用
奈米線蛋白質晶片
隨著奈米科技與半導體技術的進步,奈米線符合成本效益生產且高敏感的特性,若能運用在蛋白質晶片上,將可節省蛋白質使用量,降低成本並且縮短檢測時間。但過去奈米線技術無法應用於生醫檢測,主要原因為固定在奈米線上的蛋白質,因不規則排列導致抓取標的物後,產生的信號太微弱,造成檢測結果不穩定而無法被廣泛應用。
透過陳惠民研究團隊新開發的 EOP 技術,將蛋白質依設定方向固定在晶片奈米線上,並找出最適合角度使蛋白質能精準地與標的物質結合,即可提升信號強度,有效增加檢測穩定度,降低成本並節省檢測時間,應用於癌症及過敏疾病等檢測,讓奈米線蛋白質晶片更具競爭優勢。
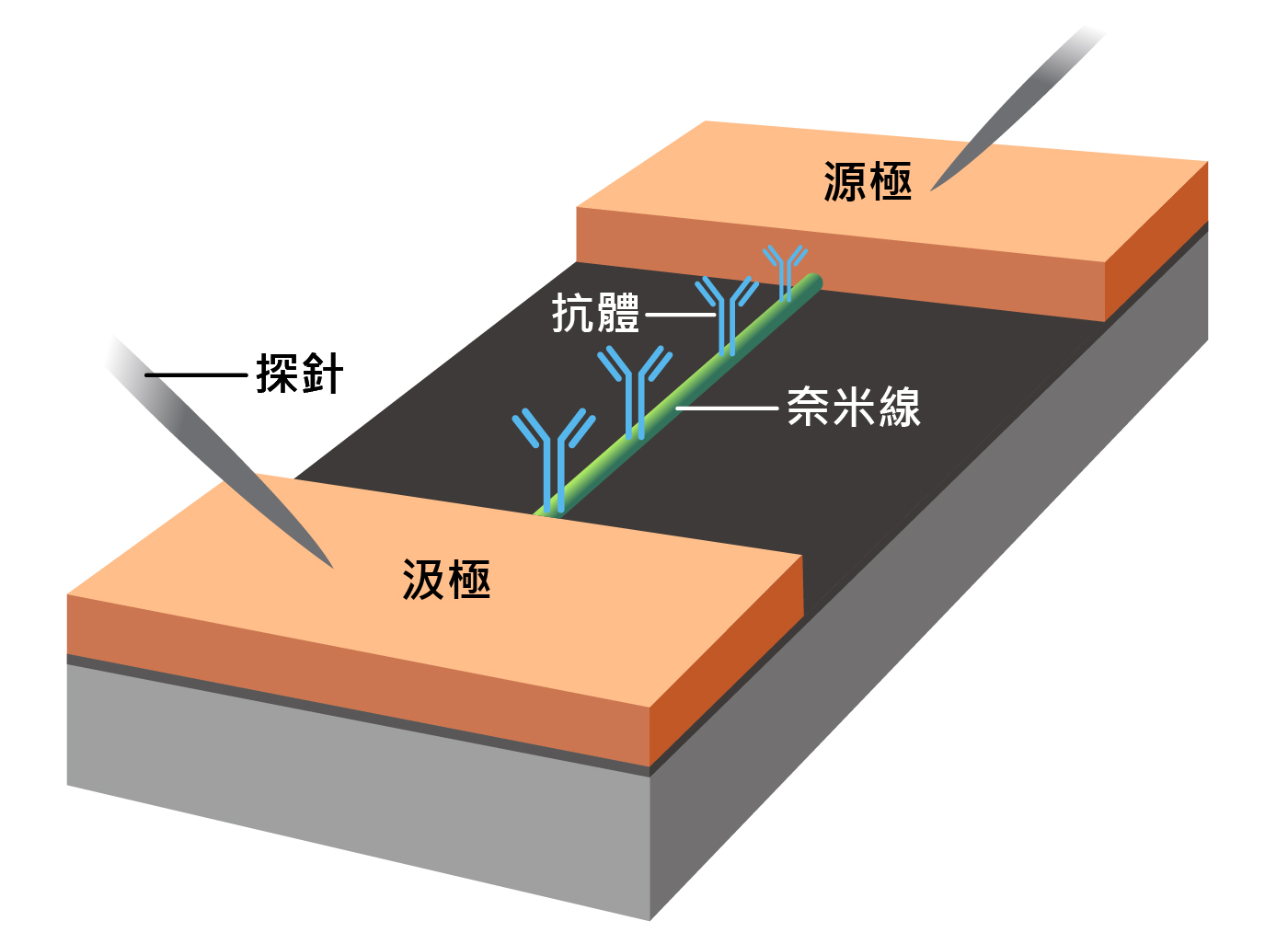
圖二:抗體透過 EOP 技術「有志一同」的固定在晶片奈米線上,更有效率地與標的物質結合,提高檢測效能。 圖/國立科學工藝博物館
晶片固定化蛋白質動態擷取技術
EOP 技術運用於蛋白質晶片,除了應用在疾病檢測,對新藥開發也極具潛力。把藥物鎖定對付目標蛋白質或細胞表面受體固定於晶片上,利用受體蛋白與配體間的專一性結合,就能夠有效率的篩選具有療效的候選藥物分子。例如中草藥的某些成分可能是與蛋白質受體的特異性配體,科學家僅需將蛋白質受體固定於晶片上,當受體蛋白與中草藥的特異性配體結合,即可從晶片分離出中草藥有效成分的萃取物。,成為新藥開發的生力軍。
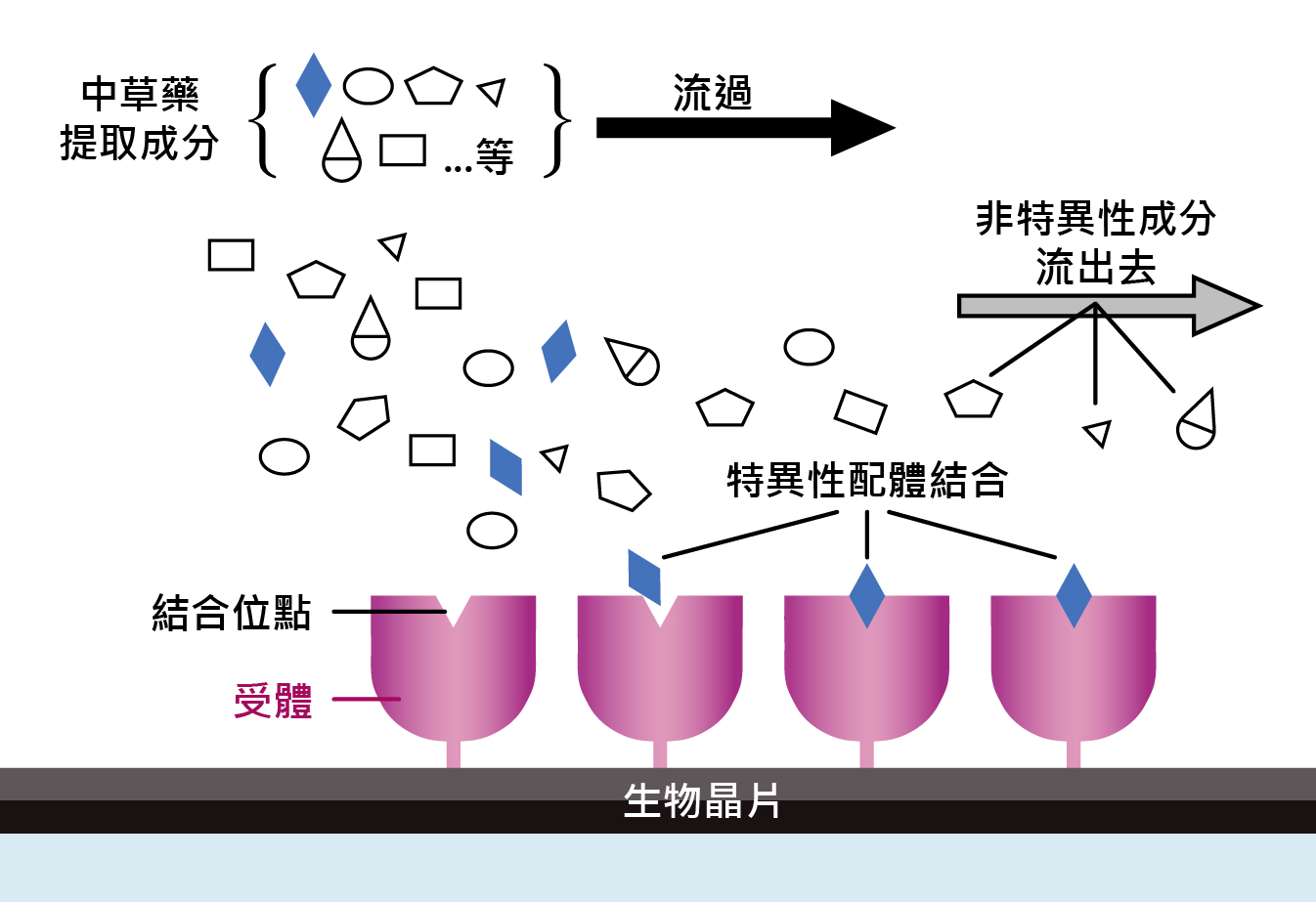
圖三:晶片固定化蛋白質動態擷取示意圖。圖/重繪自陳惠民、張哲魁,2007
陳惠民指出,台灣是全球半導體晶片世界工廠,若能利用半導體產業技術優勢發展生物醫學晶片,必能發揮「1+1>2」的加乘效果,帶動我國生技醫藥產業發展,在生物醫學檢驗與新藥開發扮演舉足輕重的角色,提升人類健康福祉。
本著作係採用 創用 CC 姓名標示─非商業性─禁止改作 3.0 台灣 授權條款 授權.
本授權條款允許使用者重製、散布、傳輸著作,但不得為商業目的之使用,亦不得修改該著作。 使用時必須按照著作人指定的方式表彰其姓名。
閱讀授權標章或
授權條款法律文字。