探究題目與動機
今年寒假後又發生 A 型流感,學校有很多同學都因為發高燒而住院,有些同學為 A 型流確認案例,還要在家裡自我隔離 5 天,學校更為此幾乎每個星期都要用漂白水(次氯酸鹽)做消毒。 而學務處衛生組長和護士阿姨要求我們要天天量體溫,每天額溫槍在額頭”開一槍”感覺有點……,若有人感染 A 型流感,會不會讓病毒傳播到下一個人身上,於是我們班導就每個人發給我們一張額溫貼片,額溫貼片有一個有趣的現象,就是放到額頭時會變色,發燒的人變色的比沒發燒的人變色多一個格子,如此來分辨這個同學是否需要回家隔離。為什麼額溫貼片有這樣神奇的現象?
這時我們剛好想起有一次班上同學一起參觀綠色博覽會時,我們發現一個表演魔術的人,手上的紙牌是牌上面的心與方塊是粉紅色的,但是用手搓一搓竟然變成藍色,好神奇!! 我們自然老師在場說:「這個我也會,這樣的表演是國中自然與生活科技第三冊,熱對物質的影響,回去看看氯化亞鈷或硫酸銅,或許可以找到一些線索」。
因為好奇心,讓這件往事回到腦海中,再詢問過老師與上網搜尋額溫貼片後,才知這是一種類似”液晶”受到溫度的影響所產生的變化,但是網路上並沒有很足夠的資訊,我們於是依據以往學過的一些簡單的實驗為基礎,設計一連串的實驗進行探討,以便探討還有什麼方式可得知溫度變化與顏色變化的關係。
相關原理
(一)自然與生活科技課本在溫度與物質變化的單元,提到含水的氯化亞鈷脫水後會由粉紅色轉變成藍色,而脫水可藉由加熱來進行反應,而吸水現象則將無水氯化亞鈷由藍色轉變成粉紅色,會放出熱量,故溫度會影響到含水氯化亞鈷的顏色,或可說溫度可以影響含水氯化亞鈷的平衡,含水硫酸銅也有類似的情形,藍色含水硫酸銅加熱脫水後轉變成白色無水硫酸銅,白色無水硫酸銅脫水後轉變成藍色含水硫酸銅並放熱。
反應式:
CoCl2(藍色無水硫酸銅)+ XH2O <=> CoCl2.XH2O(粉紅色含水硫酸銅)
CuSO4(白色無水硫酸銅)+ XH2O <=> CuSO4.XH2O(藍色含水硫酸銅)
(二)氯化亞鈷與硫酸銅微溶於乙醇,微溶於甲醇等有機化合物,容易溶於水、氨水。不同的液體與水會有不同的互溶性,有些易溶如乙醇,有些難溶如乙酸乙酯,所以不同的液體會因氯化亞鈷或硫酸銅與競爭與水分子結合,而使得氯化亞鈷或硫酸銅脫水或水合(改變結晶水的含量)而變色,不同的混合溶液比例不同脫水效果(所含的結晶水個數減少量)也不同,故會影響其溶液顏色。
(三)可逆反應在不同溫度之下,會改變不同的反應狀態,如自然與生活科技課本中提到的二氧化氮及四氧化二氮的平衡狀態,改變溫度就會改變顏色的深淺,這也說明氯化亞鈷或硫酸銅的不同液體的混合溶液含水與不含水的(結晶水個數的變化)平衡會被溫度影響而改變其顏色。
探究目的與假設
(一)探討固定用量的含水氯化亞鈷(粉紅色)在不同混合溶液的不同比例下的顏色變 化。
(二)將氯化亞鈷各種不同混合溶液的不同比例加熱並觀察溫度與其顏色變化。
(三)探討固定用量的含水硫酸銅(藍色)在各種不同混合溶液之不同比例顏色變化。
(四)將硫酸銅各種不同混合溶液的不同比例加熱並觀察其顏色變化。
(五)利用自製測量裝置,觀察最佳顏色變化的混合溶液不同混合溶液的不同比例(乙醇效果佳又容易取得以乙醇和水 9:1 加入氯化亞鈷為最佳混合液及混合比例)下 的顏色變化與電阻改變的關係。
探究方法與驗證步驟
儀器與藥品?
(一)藥品:
含水氯化亞鈷 一瓶、含水硫酸銅 一瓶、甲醇 一瓶、乙醇 一瓶、丙醇 一瓶、丙酮 一瓶、氨水 一瓶、鹽酸 一瓶
(二)器材:
試管 十支、試管架 一個、溫度計 三支、玻璃棒 六支、燒杯(500mL) 四個、滴管 六支、量筒(10mL) 四個、加熱裝置 一組、雷射光筆 一支、樂高積木 適量、黑色不反光絨布紙 一大張
(一)配製含水氯化亞鈷各種溶液之不同比例的水溶液。
(甲醇,乙醇,丙醇,丁醇,丙酮,氨水,鹽酸水溶液)
1、分別在試管中加入水:10、9、8、7、6、5、4、3、2、1、0(ml)及約 0.6 克的 氯化亞鈷並加以攪拌使盡可能溶解。
2、而後分別在試管中加入甲醇:0、1、2、3、4、5、6、7、8、9、10(ml) 並加以攪拌。
3、由室溫開始(約攝氏 25 度),放在恆溫槽中加熱,每隔攝氏 5 度觀察並記 3 錄其顏色的變化。
4、由於丙酮的沸點攝氏 56.5 度,及甲醇的沸點攝氏 64.7 度,所以加熱溫度 已不超過丙酮沸點為最高溫,以免丙酮因為沸騰而導致液體噴出,影響實 驗的準確性。
5、將甲醇改成、乙醇、丙醇、丁醇、丙酮、氨水、鹽酸等液體重複上述步驟 1、 2、3、4。
 氯化亞鈷加熱圖一。氯化亞鈷加熱圖二
氯化亞鈷加熱圖一。氯化亞鈷加熱圖二(二)配製含水硫酸銅各種溶液之不同比例的水溶液。
(甲醇,乙醇,丙醇,丁醇,丙酮,氨水,鹽酸水溶液)
1、分別在試管中加入水:10、9、8、7、6、5、4、3、2、1、0(ml)及約 0.6 克的 硫酸銅並加以攪拌使盡可能其溶解。
2、而後分別在試管中加入甲醇:0、1、2、3、4、5、6、7、8、9、10(ml) 並加以攪拌。
3、由室溫開始(約攝氏 25 度),放在恆溫槽中加熱,每隔攝氏 5 度觀察並記 錄其顏色的變化。
4、由於丙酮的沸點攝氏 56.5 度,及甲醇的沸點攝氏 64.7 度,所以加熱溫度 已不超過丙酮沸點為最高溫,以免丙酮因為沸騰而導致液體噴出,影響實 驗的準確性。
5、將甲醇改成、乙醇、丙醇、丁醇、丙酮、氨水、鹽酸等液體重複上述步驟 1、 2、3、4。
(三)利用乙醇與水 9:1(9mL 乙醇+1mL 水)加入 0.6g 氯化亞鈷,並加以攪拌,由室溫開 始(約攝氏 25 度),放在恆溫槽中加熱,每隔攝氏 5 度觀察並將其放入測量電阻裝置, 求電阻與顏色變化關係。
PS:測量電阻裝置原理是利用樂高積木組成裝置,白色光源射向光敏電阻,光敏電阻中間放 置裝入特定溫度氯化亞鈷混合溶液,利用混合液不同溫度產生不同的透光量,讓光敏電 阻產生不同的電阻。
 變色溫度計測溫裝置外觀。變色溫度計測溫裝置內部
變色溫度計測溫裝置外觀。變色溫度計測溫裝置內部結論與生活應用
(一)氯化亞鈷,硫酸銅一般是用來測知”是否含有水分”,而此次實驗則是利用氯化亞鈷, 硫酸銅顏色的改變來測知”溫度的變化”。
(二)本次實驗使用含水氯化亞鈷與含水硫酸銅主因,在實驗初期利用無水氯化亞鈷與無水 硫酸銅,因為宜蘭濕氣重,取藥幾次後藥品就已經部分變色,如此將影響用量,因此 最後統一改用含水化合物
(三)由實驗結果得知,可用來測量溫度變化的只有氯化亞鈷溶液,硫酸同溶液並不隨溫度 而改變顏色。
(四)其中氯化亞鈷的甲醇、乙醇、丙醇、鹽酸的某些比例的水溶液,可用來測知溫度的變化。
1.甲醇溶液中比例 1:9 的溶液,在 35~40℃由粉紅色變紫色。
2.乙醇溶液中比例 1:9 的溶液,在 35~40℃由粉紅色變淡紫。
3.(1)丙醇溶液中比例 2:8 的溶液,在 30~35℃由粉紅色變紫
3.(1)丙醇溶液中比例 2:8 的溶液,在 40~45℃由紫色變深紫
3.(1)丙醇溶液中比例 2:8 的溶液,在 65~70℃由深紫色變藍
4.(1)丙酮溶液中比例 4:6 的溶液,在 35~40℃由粉紅色變紫
5.(1)鹽酸溶液中比例 5:5 的溶液,在 30~35℃由粉紅色變紫
5.(1)鹽酸溶液中比例 5:5 的溶液,在 45~50℃由紫色變藍
5.(1)鹽酸溶液中比例 4:6 的溶液,在 45~50℃由粉紅色變紫
(五)將以上各比例的溶液加以組合,我們就可以藉由顏色都改變來測知溫度的變化。
(六)甲醇、乙醇、丙醇、丁醇、丙酮、氨水、鹽酸皆可將氯化亞鈷溶解。
(七)硫酸銅溶液無法拿來做溫度的測試,但從此實驗得知硫酸銅溶於甲醇、氨水、鹽 酸中,不溶於其他溶劑中。
(八)觀察各溶液可知,溶劑高溫時脫去氯化亞鈷中的水較脫去低溫時氯化亞鈷的水溶 液容易。
(九)照相由於於採光的問題,使得溶液顏色不易觀察辨識,故無法有效以照相為證明,最 後我們利用常見的乙醇及水溶液且乙醇與水比例為 1:9 為最佳變色劑,再利用光敏電阻 測量顏色變化(紅色與藍色的比值)。
(十)氯化亞鈷乙醇水溶液(1:9)顏色與電阻關係
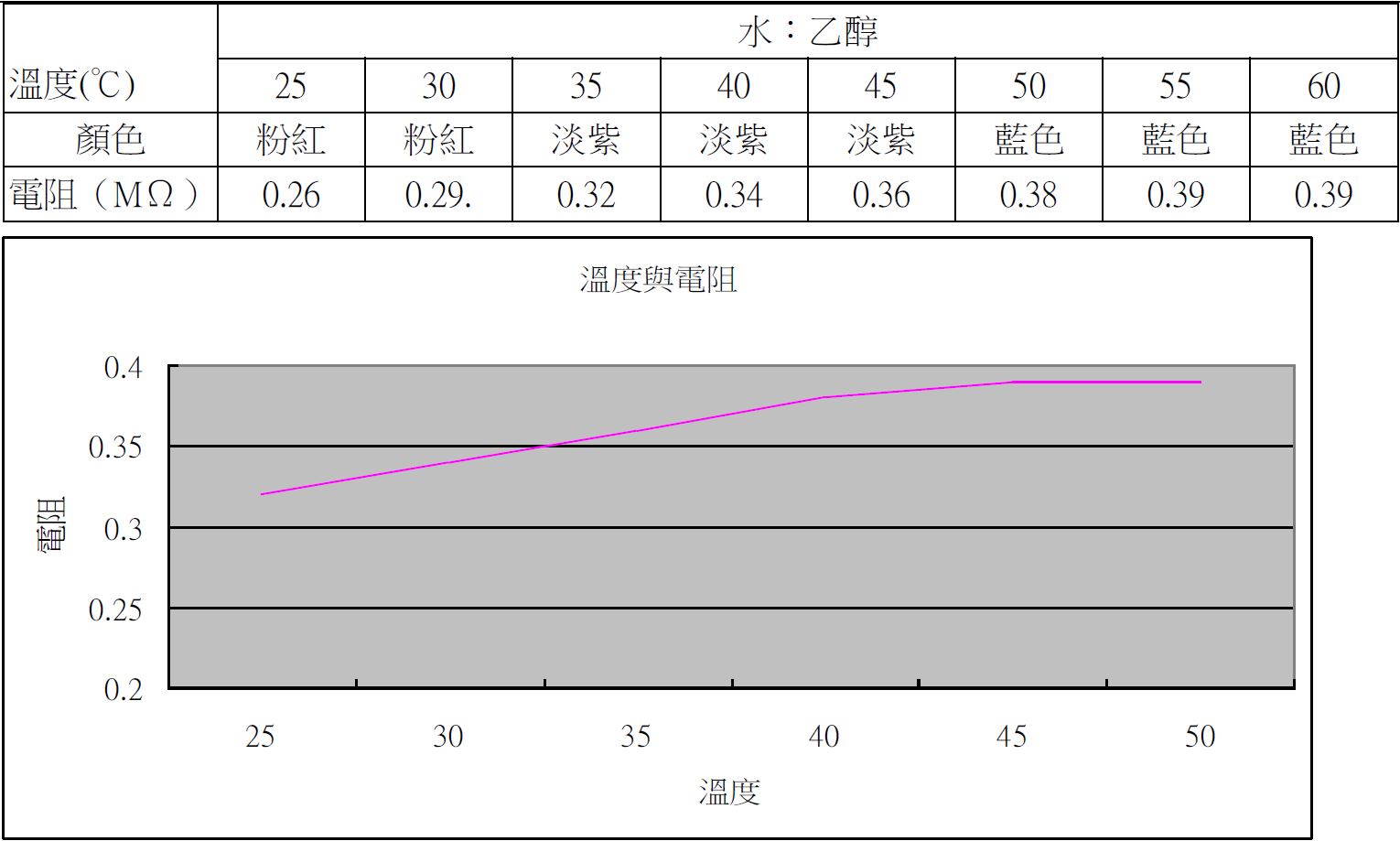 溫度與電阻圖表
溫度與電阻圖表(十一)因此我們可以推論當物質可以與硫酸銅或氯化亞鈷搶水時,可反應的物質在水與 該物質混合液中的比例越高,脫水效果越好,這應該與自然與生活科技課程中粒 子濃度越高反應碰撞機會越大就越能產生反應的現象有關。
(十二)利用最佳變色氯化亞鈷混合液,在不同溫度會產生不同電阻,這樣的電阻可以為訊 號類似車子控溫系統,等到高中職後有更多背景知識,再做後續控溫的討論。
 氯化亞鈷加熱圖一。氯化亞鈷加熱圖二
氯化亞鈷加熱圖一。氯化亞鈷加熱圖二 變色溫度計測溫裝置外觀。變色溫度計測溫裝置內部
變色溫度計測溫裝置外觀。變色溫度計測溫裝置內部 溫度與電阻圖表
溫度與電阻圖表