好萊塢賣座科幻電影「X戰警」主角金鋼狼擁有超強自癒能力,可以從各種創傷快速癒合復原。常人雖然無法像金鋼狼那般百害不侵,但成功大學研究團隊研發近紅外光照射最新療法,經動物試驗證實可加速傷口癒合。這項技術究竟是突破哪些傷口照護瓶頸?運用了哪些原理呢?
 在傷口癒合的過程中,「氧氣」都是相當關鍵的角色,因此從1960年代起,科學家開始以氧氣治療傷口。(圖/Brian Patrick Tagalog,Unsplash,https://unsplash.com/photos/Zcl9rMwflmw)
在傷口癒合的過程中,「氧氣」都是相當關鍵的角色,因此從1960年代起,科學家開始以氧氣治療傷口。(圖/Brian Patrick Tagalog,Unsplash,https://unsplash.com/photos/Zcl9rMwflmw)
傷口癒合的關鍵角色——氧氣
要提升傷口癒合速度,就得先找到關鍵影響因素。傷口癒合過程分為炎症期、增生期和成熟期等三個階段,氧氣在每個階段都是不可或缺的角色。T細胞和B細胞等免疫細胞在炎症期消耗氧氣以吞噬消滅入侵細菌,纖維母細胞則開始增生並移動到傷口處。
進入增生期後,因之前大量耗氧,組織出現短暫缺氧,纖維母細胞就吸引鄰近血管形成新血管輸送氧氣,並分泌更多膠原蛋白填補傷口;上皮細胞也開始變形移動到肉芽組織上面,將傷口覆蓋;粒線體供應細胞運作所需能量等過程,直至成熟期傷口收縮復原,都需要足夠的氧氣協助。
氧氣對傷口癒合如此重要,但受傷後,因傷口組織血管破裂,紅血球輸送氧氣的通路被阻斷,科學家於是開始思考利用氧氣治療的可行性,積極嘗試各種提高傷口組織氧氣濃度的方式。
如何運用氧氣治療傷口?
1960年代,科學家開始使用氧氣治療傷口。病患需要待在特殊的壓力艙,呼吸純氧來增加血液含氧濃度,藉此提高傷口組織的氧濃度。但這種方式不僅成本高昂,且因是全身性供氧,可能造成身體其他部位氧氣濃度過高,產生氣胸或腦血管栓塞等副作用。
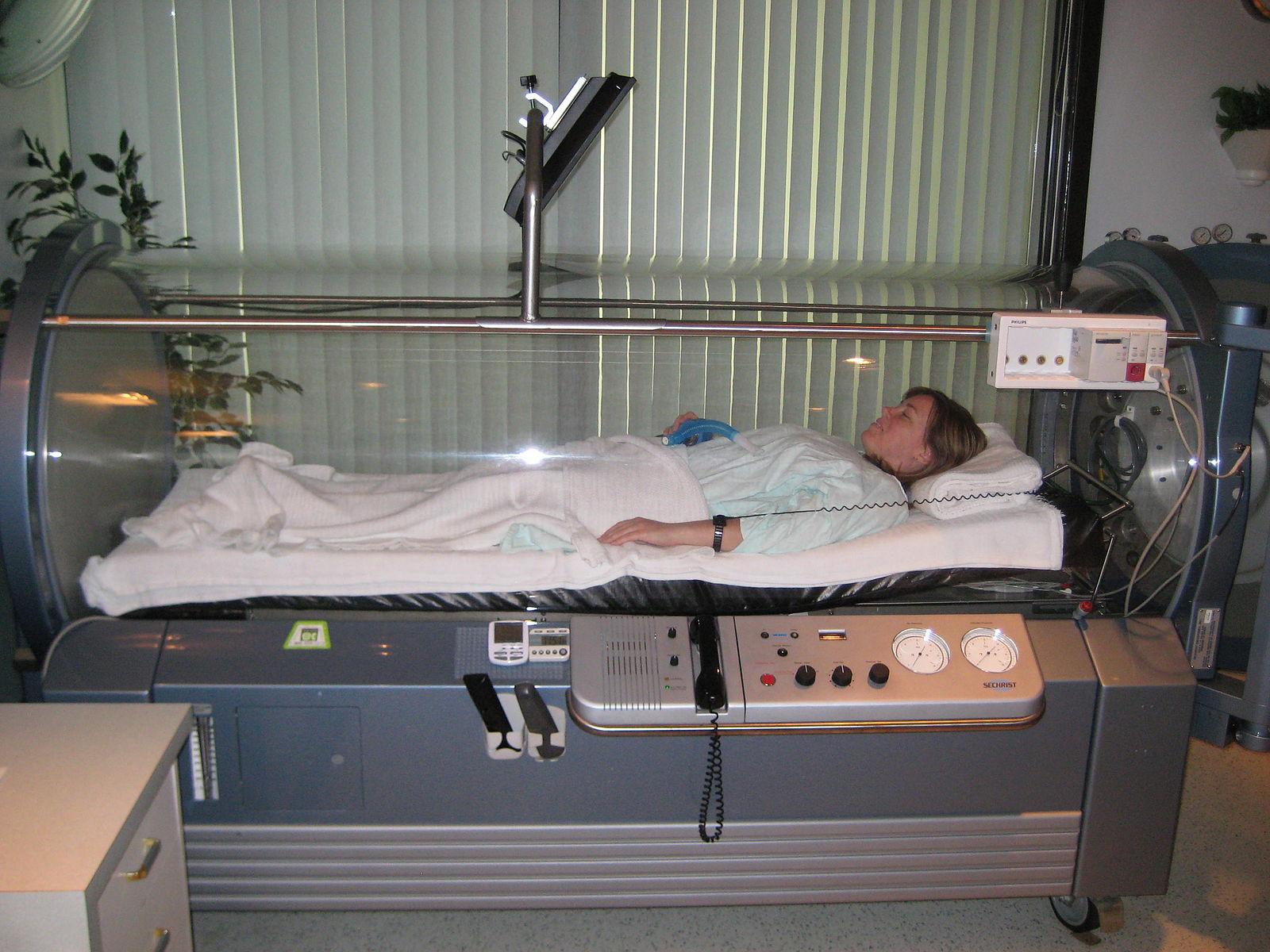 使用高壓氧療法時,病患需待在特殊的壓力艙中。(圖/James Heilman, MD ,Wikipedia)
使用高壓氧療法時,病患需待在特殊的壓力艙中。(圖/James Heilman, MD ,Wikipedia)
科學家於是改採在傷口組織局部增加氧濃度,避開高壓氧治療風險,降低醫療成本,機動性也高。但氧氣難溶於水,無法抵達傷口深處,對較深傷口療效有限。為達到局部增加氧氣濃度,又能讓深入傷口組織,就必須克服水溶性的問題。科學家也因此把腦筋動到二氧化碳身上!
二氧化碳神奇的波爾效應
大家都知道二氧化碳是造成溫室效應的兇手,但對傷口癒合卻是神奇救兵。1904年丹麥生理學家克里斯蒂安.波爾(Christian Bohr)提出「波爾效應」,證實透過紅血球調節血液酸鹼值,提高二氧化碳濃度,讓血液酸鹼值偏酸,便能促使血紅素釋出氧氣。
二氧化碳療法便是運用「波爾效應」,促使血紅素在肌肉組織及末梢組織釋放出更多氧氣,活化細胞並促進血液循環,已被證實能促進新陳代謝和組織再生。療法是把少量二氧化碳,經過皮内或皮下注射到體内,誘發局部區域產生較高濃度氧氣,藉此治療傷口。
奈米光療癒合效果加乘
「波爾效應」為傷口治療開啟新窗,成功大學化學系講座教授葉晨聖則帶領研究團隊,結合近紅外光與奈米藥劑,讓二氧化碳療法更上層樓。經小鼠試驗顯示,傷口接受五分鐘照射治療,癒合時間就可縮短三分之一。
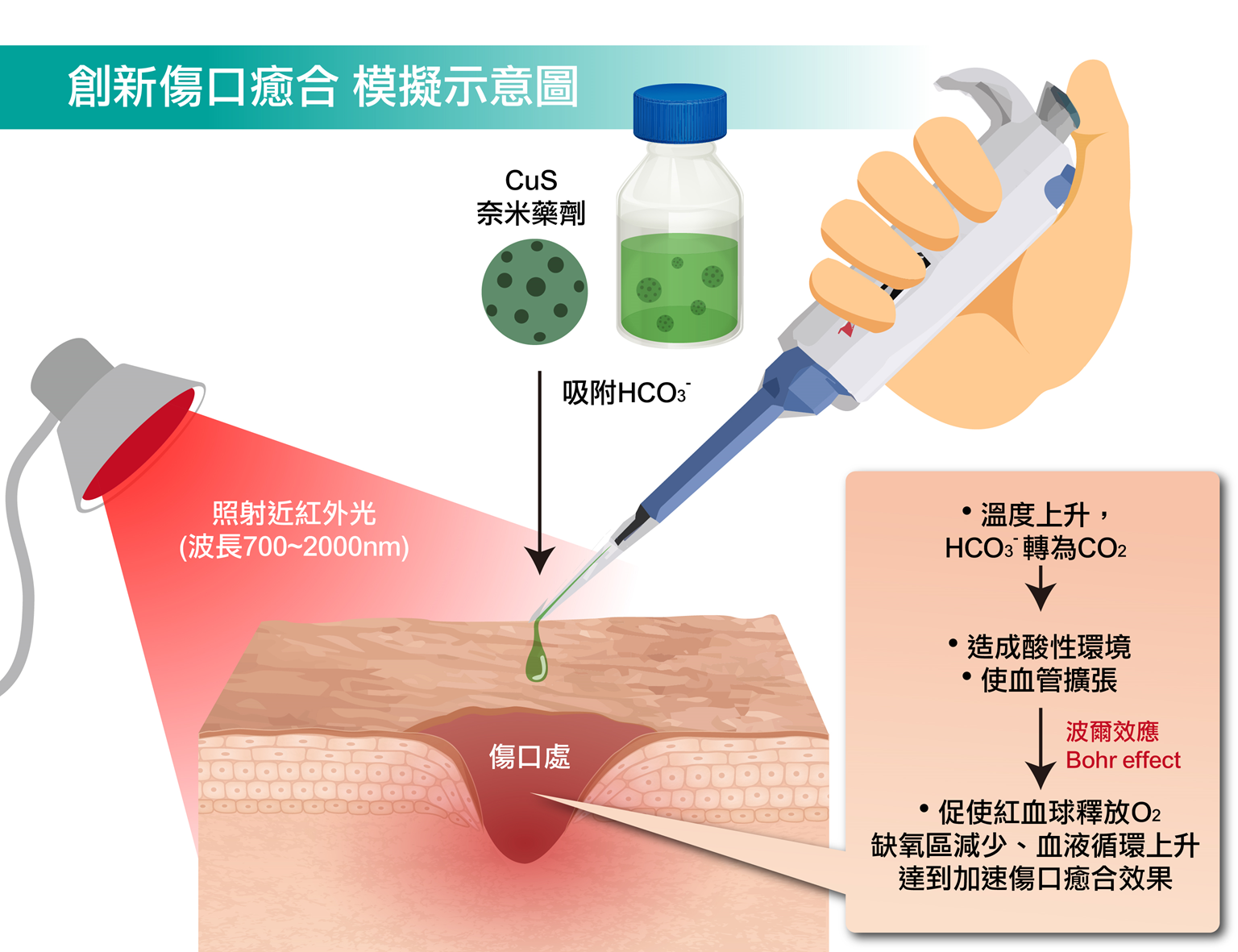 硫化銅粒子吸附小蘇打粒子,透過近紅外光照射,小蘇打粒子遇熱產生二氧化碳,傷口環境轉變成弱酸性,觸發波爾效應,提高傷口氧氣濃度,加速傷口癒合。(圖/國立科學工藝博物館提供)
硫化銅粒子吸附小蘇打粒子,透過近紅外光照射,小蘇打粒子遇熱產生二氧化碳,傷口環境轉變成弱酸性,觸發波爾效應,提高傷口氧氣濃度,加速傷口癒合。(圖/國立科學工藝博物館提供)
研究團隊把硫化銅奈米粒子孔洞化,增加接觸表面積,裡外吸附碳酸氫鈉(NaHCO3
,俗稱小蘇打),製作成奈米藥劑。在小鼠背部劃出2公分傷口,把藥劑滴在傷口表面,再用波長700-2000奈米近紅外光照射約五分鐘,當藥劑溫度升高至攝氏40-42度左右,小蘇打受熱分解產生二氧化碳,促使血液酸鹼值轉為弱酸性,進而誘發血紅素釋出氧氣。
研究團隊追蹤小鼠傷口組織血液循環及癒合狀況,發現藥劑釋出的二氧化碳,不但使血管擴張,促進血液循環,更令人驚豔的是「波爾效應」的加乘效果,進行一次性的五分鐘治療,便可讓傷口癒合時間從三周縮短至兩周。
葉晨聖研發的奈米藥劑,不但順利解決傳統氧療法的溶氧障礙,也成功改善二氧化碳侵入性療法的疼痛問題。研究團隊預定把奈米藥劑進一步從滴劑轉化成貼片,讓傷口治療能更簡易且迅速。
 在傷口癒合的過程中,「氧氣」都是相當關鍵的角色,因此從1960年代起,科學家開始以氧氣治療傷口。(圖/Brian Patrick Tagalog,Unsplash,https://unsplash.com/photos/Zcl9rMwflmw)
在傷口癒合的過程中,「氧氣」都是相當關鍵的角色,因此從1960年代起,科學家開始以氧氣治療傷口。(圖/Brian Patrick Tagalog,Unsplash,https://unsplash.com/photos/Zcl9rMwflmw) 使用高壓氧療法時,病患需待在特殊的壓力艙中。(圖/James Heilman, MD ,Wikipedia)
使用高壓氧療法時,病患需待在特殊的壓力艙中。(圖/James Heilman, MD ,Wikipedia) 硫化銅粒子吸附小蘇打粒子,透過近紅外光照射,小蘇打粒子遇熱產生二氧化碳,傷口環境轉變成弱酸性,觸發波爾效應,提高傷口氧氣濃度,加速傷口癒合。(圖/國立科學工藝博物館提供)
硫化銅粒子吸附小蘇打粒子,透過近紅外光照射,小蘇打粒子遇熱產生二氧化碳,傷口環境轉變成弱酸性,觸發波爾效應,提高傷口氧氣濃度,加速傷口癒合。(圖/國立科學工藝博物館提供)