 (圖/Zoltan Tasi提供,Unsplash)
(圖/Zoltan Tasi提供,Unsplash)阿黴素是什麼?
阿黴素Doxorubicin(簡稱Dox,結構如下圖)是一種抗癌藥物,被用在許多不同的癌症治療上,例如乳腺癌、卵巢癌、胃癌、甲狀腺癌、多發性骨髓瘤、淋巴瘤、急性淋巴細胞白血病(ALL)、急性髓細胞白血病(AML)……等,都會利用Dox進行化學療法。由於藥物本身無法區別癌細胞和正常細胞,所以會同時攻擊兩者,導致身體虛弱而出現嘔吐、掉髮等化療副作用;因此,把Dox與DNA適體的功能結合,就可以讓Dox只針對癌細胞發揮作用。
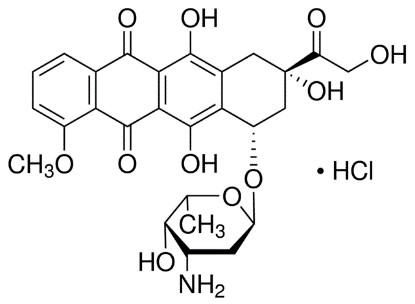 阿黴素Doxorubicin(簡稱Dox)化學結構式。(圖/林泱蔚教授團隊提供)
阿黴素Doxorubicin(簡稱Dox)化學結構式。(圖/林泱蔚教授團隊提供)金奈米粒子搭配Dox與DNA適體最剛好
想讓Dox與DNA適體共同發生作用,就要把這兩種物體放在一起。可以把金奈米粒子的hairpin DNA (簡稱hpDNA)想像成飛碟,飛碟上的座位大小是0.34nm,而Dox大小剛好也是0.34 nm,因此作為乘載Dox的交通工具,hpDNA再適合不過了!但是,hpDNA並不如想像中完美,雖然剛好可以乘載藥物,卻沒有定位的能力,會像迷航在宇宙中的飛碟找不到目的地,一不小心還會傷害到健康的細胞。因此,DNA適體就負責在航程中擔任GPS的角色,帶領飛碟抵達目的地(癌細胞)。
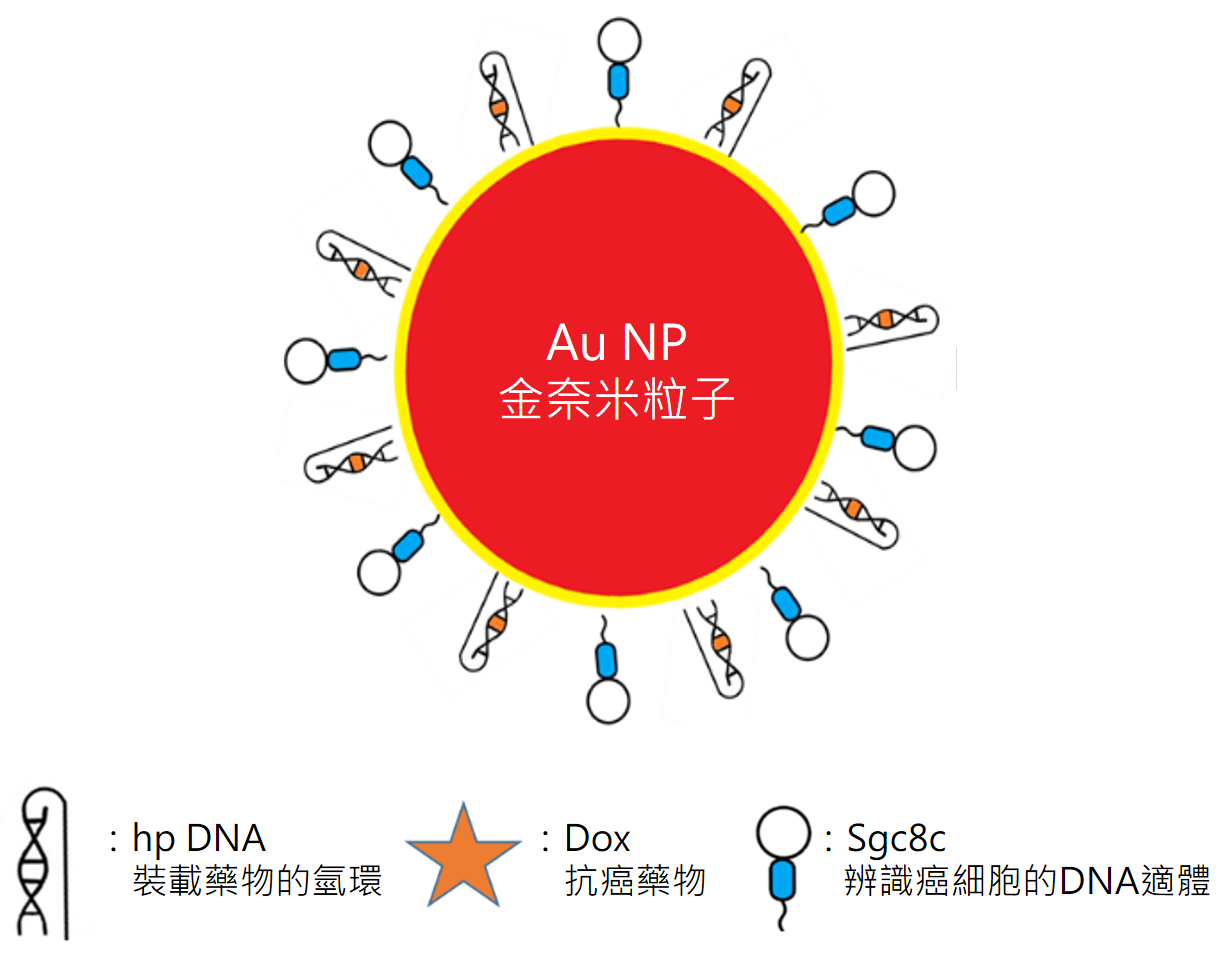 金奈米粒子(Au NP)裝載Sgc8c(DNA適體)、hpDNA、Dox抗癌藥物的方式。此種藥物裝載方式會以金奈米粒子的hairpin DNA (簡稱hpDNA)為核心裝載Dox藥物,再加上能辨識癌細胞的 Sgc8c適體。(圖/林泱蔚教授團隊提供)
金奈米粒子(Au NP)裝載Sgc8c(DNA適體)、hpDNA、Dox抗癌藥物的方式。此種藥物裝載方式會以金奈米粒子的hairpin DNA (簡稱hpDNA)為核心裝載Dox藥物,再加上能辨識癌細胞的 Sgc8c適體。(圖/林泱蔚教授團隊提供)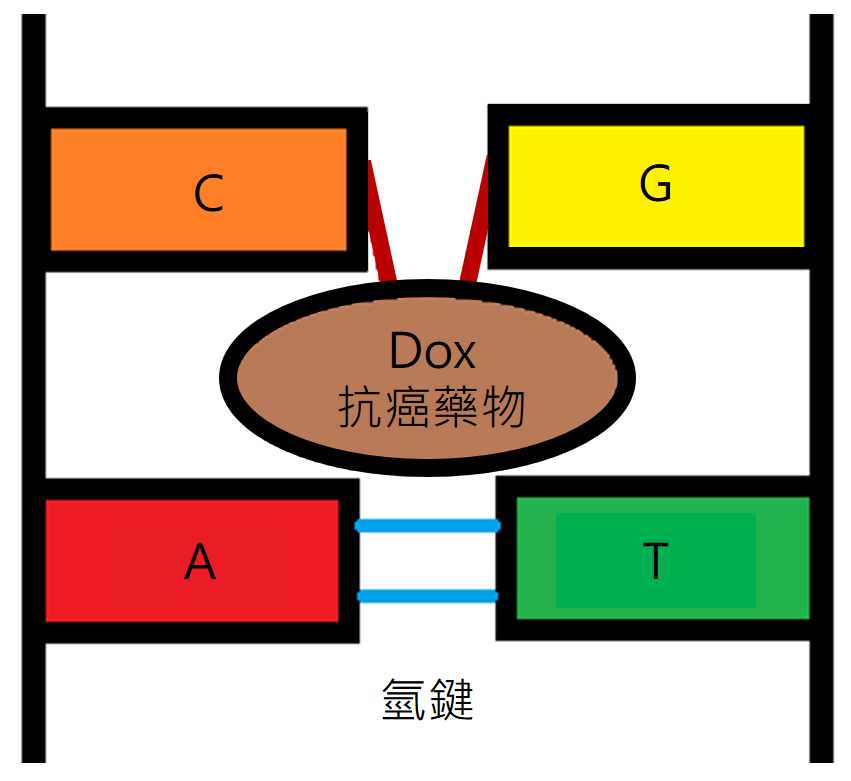 hpDNA與Dox裝載情形,可以想像成是飛碟的座位圖,Dox的大小剛好與座位大小相符。(圖/林泱蔚教授團隊提供)
hpDNA與Dox裝載情形,可以想像成是飛碟的座位圖,Dox的大小剛好與座位大小相符。(圖/林泱蔚教授團隊提供)為什麼選擇金奈米粒子?
在眾多粒子當中,選擇金奈米粒子的理由是,金奈米粒子在接受特定波長的光(532 nm)照射後會釋放出熱,放出的熱就會破壞hpDNA與金奈米粒子之間的連接,進而釋放出Dox抗癌藥物,這個接受光、放出熱、破壞連接的過程就稱為光活化。可以想像成光就是開啟飛碟的按鈕,照光之後飛碟的門會打開,座位裡的Dox藥物才能被釋放出來殺死癌細胞。
目前科學家把找到癌細胞的GPS (DNA適體)稱為Sgc8(註1),這個序列對於人類急性淋巴性白血病T淋巴細胞系(註2)上的特殊蛋白「protein tyrosine kinase 7 (簡稱PTK7)」有很高的結合力,會主動鍵結到癌細胞上,當Sgc8c找到PTK7以後,就可以釋放藥物。
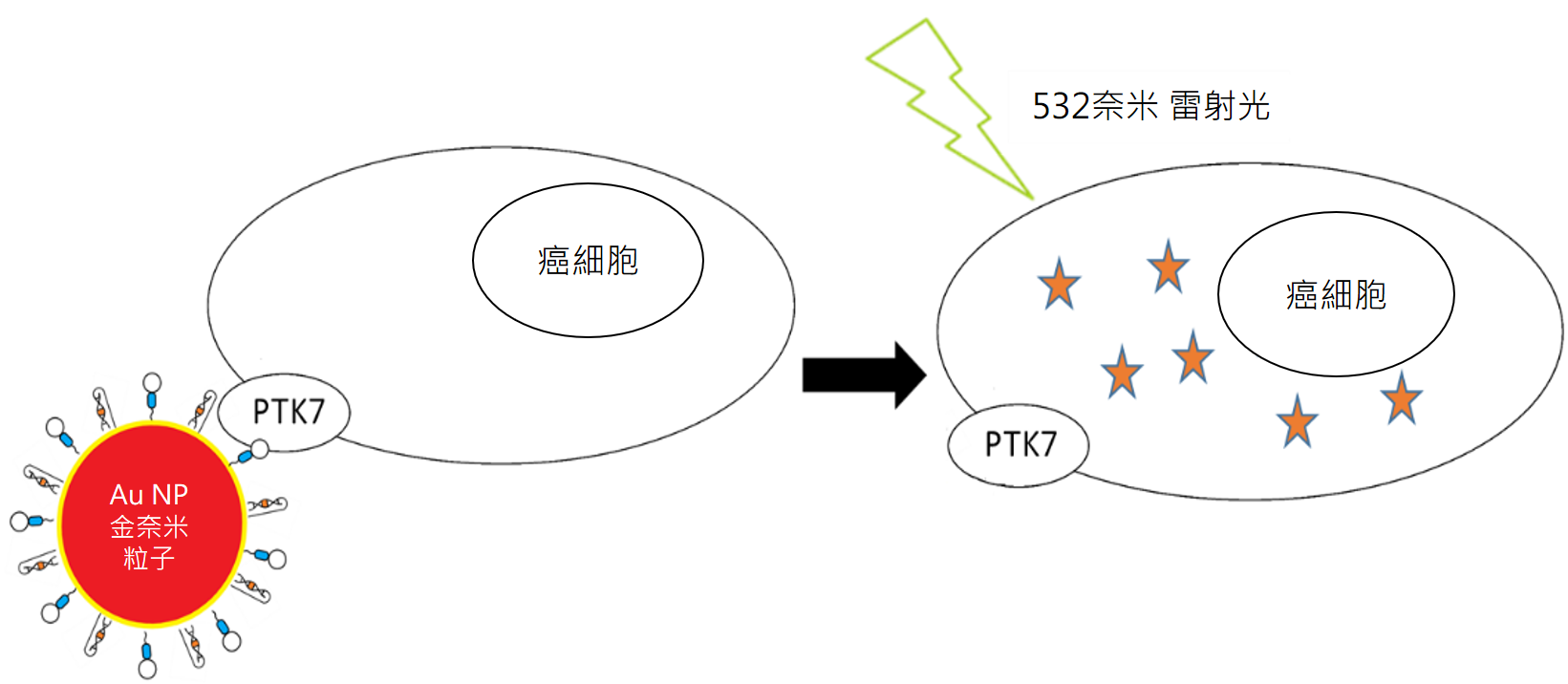 金奈米粒子受到光活化作用後釋放Dox藥物的流程。可以想像成裝載抗癌藥物的飛碟,透過DNA適體的導航找到包覆癌細胞的特殊蛋白PTK7,之後照光,就能打開飛碟的門讓Dox藥物釋出殺死癌細胞。(圖/林泱蔚教授團隊提供)
金奈米粒子受到光活化作用後釋放Dox藥物的流程。可以想像成裝載抗癌藥物的飛碟,透過DNA適體的導航找到包覆癌細胞的特殊蛋白PTK7,之後照光,就能打開飛碟的門讓Dox藥物釋出殺死癌細胞。(圖/林泱蔚教授團隊提供)光活化過程是透過電子分布達到放熱效果
光活化的過程是怎麼進行的呢?前面提到金奈米粒子在吸收特定波長的光後會釋放出熱,而導致金奈米粒子放熱的原因是「表面電漿共振效應」。所謂的表面電漿共振效應指的是,金屬奈米粒子在受到光的影響以後,表面的電漿會產生電子分布不均勻的狀況,電子少的地方會吸引電子,電子多的地方會排斥電子,在吸引、排斥的作用下,就會讓金屬奈米粒子放熱,導致原先在金屬奈米粒子上的鍵結斷裂、釋放藥物。
 彰化師範大學教授林泱蔚的團隊利用紫色雷射光照射亞甲藍溶液的呈色反應,模擬模擬光熱效應釋放出hpDNA上的Dox抗癌藥物。 (A)未照光的亞甲藍與還原劑作用,生成無色的還原態(B)照射紫光雷射的亞甲藍呈現出藍色。(圖/林泱蔚教授團隊提供)
彰化師範大學教授林泱蔚的團隊利用紫色雷射光照射亞甲藍溶液的呈色反應,模擬模擬光熱效應釋放出hpDNA上的Dox抗癌藥物。 (A)未照光的亞甲藍與還原劑作用,生成無色的還原態(B)照射紫光雷射的亞甲藍呈現出藍色。(圖/林泱蔚教授團隊提供)金奈米材料/Dox抗癌藥物之光熱精準治療
根據研究報告〈Y.L. Luo, Y.S. Shiao, and Y.F. Huang, “Release of Photoactivatable Drugs from Plasmonic Nanoparticles for Targeted Cancer Therapy”, ACS Nano, 2011, 5, 7796-7804.〉的結果顯示,該研究所開發的Sgc8c/hp-Au NP,不僅增加對目標細胞的選擇性以及控制藥物的精確釋放,且金奈米粒子是細胞毒性較低的奈米材料,可在532 nm的光照射下,表現出高效的光熱效應,相較於過往的癌症治療,具有顯著的治療效果。
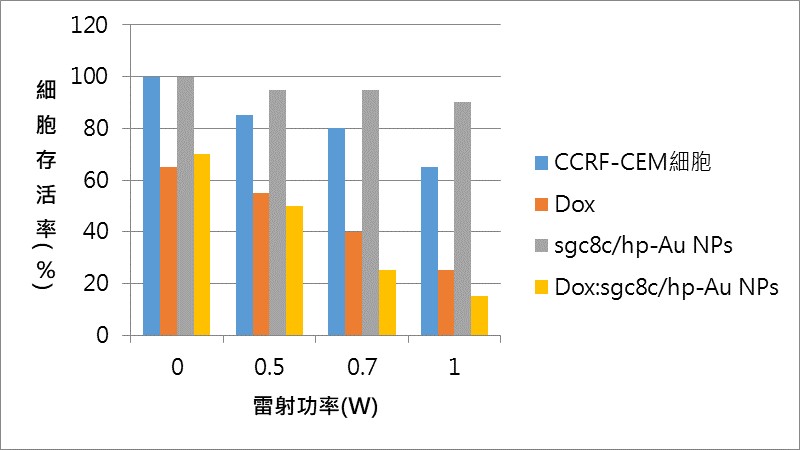 人類急性淋巴性白血病T淋巴細胞(CCRF-CEM)容易受到光熱毒殺效果(黃色柱狀),本身也會因為光熱而降低存活率(藍色柱狀)。然而,如果只用Sgc8c/hp-Au NPs(金奈米粒子,灰色柱狀)而不搭配Dox治療,光熱毒殺效果不明顯,表示金奈米粒子本身對CCRF-CEM細胞有吸收光能量保護效應,因此療效反而會降低。(圖∕黃郁棻教授團隊提供實驗數據,林泱蔚教授團隊重繪)
人類急性淋巴性白血病T淋巴細胞(CCRF-CEM)容易受到光熱毒殺效果(黃色柱狀),本身也會因為光熱而降低存活率(藍色柱狀)。然而,如果只用Sgc8c/hp-Au NPs(金奈米粒子,灰色柱狀)而不搭配Dox治療,光熱毒殺效果不明顯,表示金奈米粒子本身對CCRF-CEM細胞有吸收光能量保護效應,因此療效反而會降低。(圖∕黃郁棻教授團隊提供實驗數據,林泱蔚教授團隊重繪)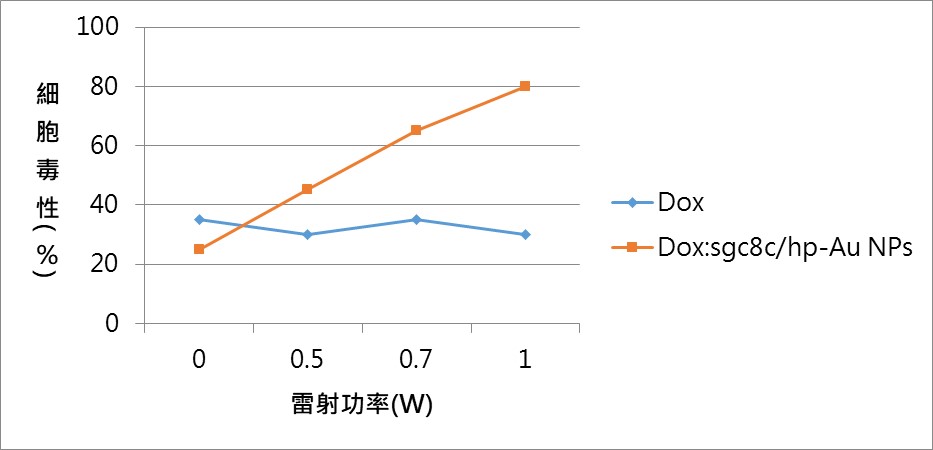 上圖所呈現的是在不同雷射功率之下藥物能釋放出多少殺死癌細胞的毒性,如果只有Dox,本身釋放的毒性不會隨著功率增加而有顯著的提升(如藍線所示),但如果是以飛碟的形式將Dox裝載於Sgc8c/hp-Au NPs則與功率成正比(如橘線所示),隨著功率提升,會釋放越多的毒性殺死癌細胞。(圖∕黃郁棻教授團隊提供實驗數據,林泱蔚教授團隊重繪)
上圖所呈現的是在不同雷射功率之下藥物能釋放出多少殺死癌細胞的毒性,如果只有Dox,本身釋放的毒性不會隨著功率增加而有顯著的提升(如藍線所示),但如果是以飛碟的形式將Dox裝載於Sgc8c/hp-Au NPs則與功率成正比(如橘線所示),隨著功率提升,會釋放越多的毒性殺死癌細胞。(圖∕黃郁棻教授團隊提供實驗數據,林泱蔚教授團隊重繪)本著作係採用 創用 CC 姓名標示─非商業性─禁止改作 3.0 台灣 授權條款 授權.
本授權條款允許使用者重製、散布、傳輸著作,但不得為商業目的之使用,亦不得修改該著作。 使用時必須按照著作人指定的方式表彰其姓名。
閱讀授權標章或
授權條款法律文字。