 2018年諾貝爾化學獎得獎人阿諾德、史密斯和溫特教授們的研究創造了演化在應用化學領域的全新舞台,利用他們的技術及概念延伸,可擴及有利於環境、綠能源、藥物的研究,以解決空汙、能源危機、癌症等備受矚目的議題。
2018年諾貝爾化學獎得獎人阿諾德、史密斯和溫特教授們的研究創造了演化在應用化學領域的全新舞台,利用他們的技術及概念延伸,可擴及有利於環境、綠能源、藥物的研究,以解決空汙、能源危機、癌症等備受矚目的議題。
「達爾文先生,由於您在生物演化理論的傑出貢獻,恭喜您得到2018年諾貝爾化學獎(
註1)。」
電話這頭的達爾文閉上眼睛,像是再度搭上小獵犬號一般,身體不由自主地晃動著。時間彷彿隔了兩世紀那麼久,達爾文緩緩地睜開雙眼,望向窗外。「今天的陽光很耀眼。」達爾文心想,淚水在他布滿歲月的雙眸中閃閃發光。
如果達爾文在2018年慶祝他209歲生日,那這通電話達爾文是接定了。
達爾文的天擇說與人擇說
“……from so simple a beginning endless forms most beautiful and most wonderful have been, and are being, evolved” On the Origin of Species by Means of Natural Selection, or the Preservation of Favoured Races in the Struggle for Life, Charles Darwin, 1859.
達爾文以這句話做為物種原始論的結尾:「散布在地球各處美麗且多樣的生物都演化自共同而少數的生物祖先,而這樣的演化過程仍不斷進行中。」達爾文的「have been」所指的時間尺度,可以遠從太古25億年前的藍綠菌開始,這幾十億年以來,原始生命體透過天擇,逐漸從簡單的單細胞演化形成現今具豐富生物多樣性的年代。
在生物課本中,最常出現的天擇例子是長頸鹿。長頸鹿原本有長脖子和短脖子兩個品種,由於短脖子的長頸鹿吃不到高處的樹葉,只能跟矮小的動物一起搶奪低處的樹葉,因而常常餓死,在短頸鹿這個名字尚未問世前就慘遭淘汰。
達爾文除了搭乘海軍小獵犬號探索南美洲海岸外,他也是個實驗學家,他的實驗結果「The Variation of Animals and Plants Under Domestication」於1868年發表,闡述物種形成除了可透過天擇外,也可以進行人擇。人擇,就是人為選擇,或是農業上廣泛應用,稱為育種的技術,玉米是歷史上知名的人擇例子之一。
玉米是由大芻草(teosinte,蜀黍)馴化而來。在遠古時代的氣候條件下(攝氏20.1到22.5度,260 ppm的二氧化碳)生長的大芻草,形態近似於現在的玉米,不一樣的是,大芻草的種皮又硬又厚,以它做為糧食實在不好入口。藉由育種技術,挑選適合食用、可遺傳的特徵(稱為性狀),逐步把大芻草改良成種皮薄且含水量多的糧食作物。藉由人擇,人類著實在演化路上幫自己省下不少時間。
達爾文發表物種源起不到100年,在1952年證實DNA是遺傳物質,1953年提出它具雙股螺旋結構。這個重要的發現讓達爾文的論述更能清晰地從分子層級去理解及研究:DNA出現突變,突變種透過天擇或人擇達到生物繁衍的目的。
 (上)生物在地球的演化史。紫色:前寒武紀出現的生物共同祖先藍綠菌,末期遇到一次環境改變;紅色:寒武紀大爆發,現今生物的各大類別突然出現,末期環境巨大變動;綠色:進入中生代,恐龍大量出現,但後期遇到星體撞地球,溫度變化使得冷血動物接連死亡;藍色:進入新生代,鳥類哺乳類昆蟲時代,後期開始有人類出現。(下) 定向演化示意圖,演化時間尺度是數天之譜。
(上)生物在地球的演化史。紫色:前寒武紀出現的生物共同祖先藍綠菌,末期遇到一次環境改變;紅色:寒武紀大爆發,現今生物的各大類別突然出現,末期環境巨大變動;綠色:進入中生代,恐龍大量出現,但後期遇到星體撞地球,溫度變化使得冷血動物接連死亡;藍色:進入新生代,鳥類哺乳類昆蟲時代,後期開始有人類出現。(下) 定向演化示意圖,演化時間尺度是數天之譜。
阿諾德發展定向演化研究
DNA是遺傳密碼,解碼後的酵素分子就是使我們感受到生物多樣存在的主角。酵素的主體是由20種胺基酸作為單體聚合而成的生物大分子,以一個由300個胺基酸組成的酵素分子為例,可以有高達20×20×20……共乘300次個不同的排列組合(20300這個數字大到不可思議!)。
生物演化出這樣的機制,很大的優勢是可提供種類多樣的酵素分子以適應不同的生長環境,確保生物繁衍。相反地,這也成為科學家極大的挑戰——究竟人類能否發展出一套理論,正確地預測這20300個酵素分子的功能,從而設計出人工酵素供工業社會使用?
2018年諾貝爾化學獎得主阿諾德(Frances H. Arnold)教授於1987年進入加州理工學院化學工程學系擔任教職,開始研究枯草桿菌蛋白酶(subtilisin E)在有機溶劑環境中催化的能力。在生物的世界裡,水相環境就像是一預設條件,水與酵素分子的交互作用(如氫鍵)決定了酵素的立體構形,進而決定酵素催化反應的速度與專一性(事實上,在水相環境中的酵素分子並非是一硬邦邦的構形,相反地,在水相環境中的酵素分子是有彈性且隨時在變,這也是酵素與其他金屬催化劑最大不同的地方)。
為了工業上的需求,科學家發現把酵素分子置於有機溶劑環境中,由於缺少了水分子透過氫鍵對酵素分子的拉扯,有機溶劑環境提供了溫和的環境使酵素分子的構形能硬挺,大幅提升酵素結構的穩定性及酵素反應的專一性,這一特性對掌性異構物的合成特別重要。儘管有機溶劑環境對於酵素催化反應於工業應用有相當多的優點,絕大部分的酵素(包含枯草桿菌蛋白酶)在有機溶劑中並不具有催化功能(活性)(
註2)。
有別於她博士班期間專注於理論的研究(
註3),阿諾德教授認為自然是最好的化學家,她向自然取經,利用自然界的演化機制從20
300這樣的天文數字篩選出人工酵素。換言之,她引導演化的方向從而選擇出工業需要的酵素,稱為定向演化(directed evolution)。
為能做出不同排列組合的蛋白質序列,她首先以枯草桿菌蛋白酶的DNA序列作為樣板,利用隨機突變(
註4)的方式製備出枯草桿菌蛋白酶突變序列基因庫,隨後以人擇的方式挑選在有機溶劑中仍然能分解酪蛋白的枯草桿菌蛋白酶突變株,再以挑到的突變枯草桿菌蛋白酶序列作為模板,進行第二輪隨機突變及篩選。到了第三輪實驗,已經可以找出比原始的酵素在有機溶劑中的效率高出256倍的新變異種。
突變是演化的基礎,適合生存的存活了下來,經由突變而變得更適合生存。這是因為外在的因素而不得不變,科學家們就是利用這個原理,創造出人工的環境進而從突變群組中挑出適合的性狀。
阿諾德教授當時使用的技術是一項很耗工耗時的工序,她利用基本的方法,在當時分子生物技術貧乏的年代,跳脫以往框架的思考邏輯,這種模仿大自然的演化的方式,比自然的演化快上許多。她所發展的技術可應用於綠色能源及新藥開發上,如開發新酵素以加速化學反應,或避免副產物在生產過程中出現,以提升目標產物的純度。
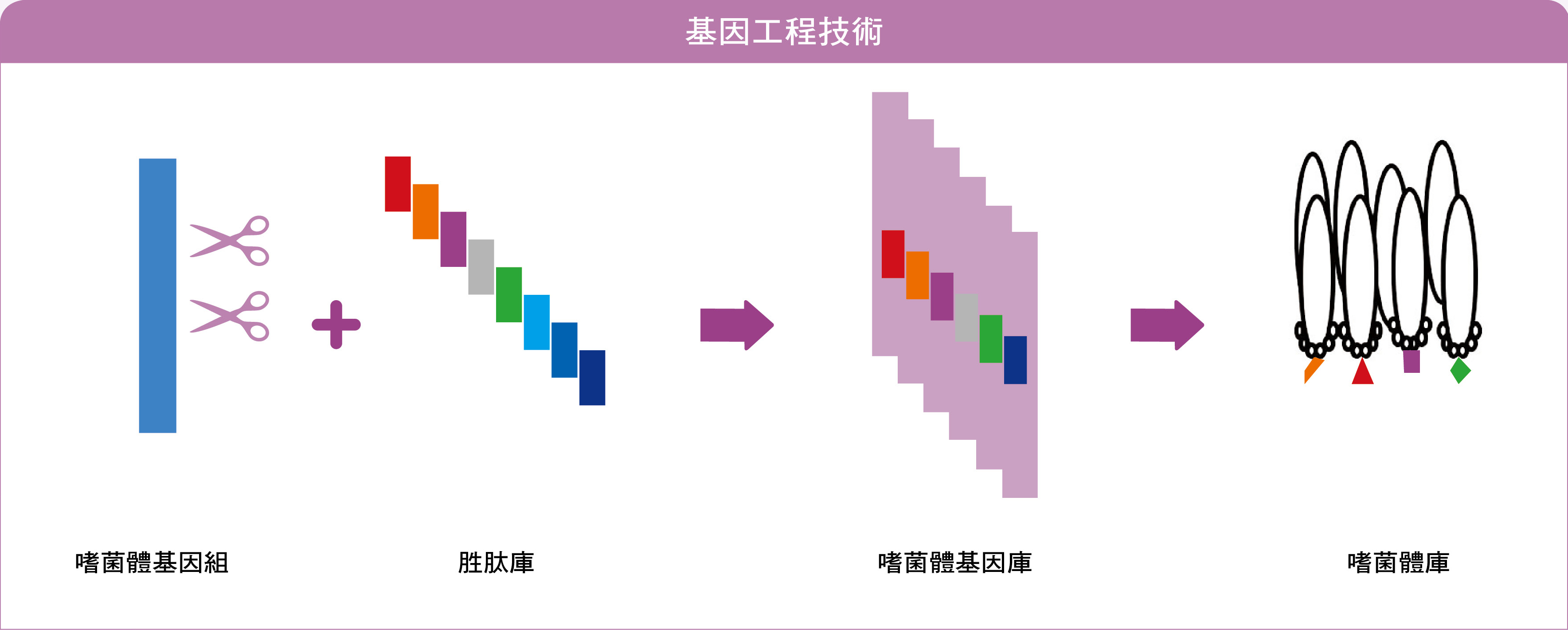 基因工程技術:利用基因工程技術把隨機突變所得到的胜肽庫嵌入噬菌體基因組得到噬菌體基因庫,進而得到表面帶有不同標籤的噬菌體庫。
基因工程技術:利用基因工程技術把隨機突變所得到的胜肽庫嵌入噬菌體基因組得到噬菌體基因庫,進而得到表面帶有不同標籤的噬菌體庫。
突變及篩選是演化的兩大基本元素,史密斯(George P. Smith)教授開發一種相當有效率的篩選工具,稱為嗜菌體展示(phage display)(
註5)。嗜菌體是一種可以感染細菌的病毒,病毒利用多個鞘蛋白所形成的複合結構裝載病毒遺傳物質。因為結構簡單,所以噬菌體相當穩定且有高度感染力,1個噬菌體經過一個晚上,可以利用寄生方式複製出1015個的噬菌體。
史密斯教授在病毒這樣簡單結構的基礎上,加入一個改變世界的小巧思,利用基因工程技術在鞘蛋白基因前嵌入一小段基因片段,讓這樣的重組基因片段能表達外源蛋白——鞘蛋白。經過實驗測試,外源蛋白既不會影響鞘蛋白本身的結構,又能讓嵌入的基因片段連同鞘蛋白一起表現在噬菌體表面,如同噬菌體被tag了。欲嵌入的基因片段可簡單地透過試管合成的方式,隨機做出不同排列組合的基因標籤庫,再利用基因工程技術嵌入噬菌體基因組內,最後得到帶有不同標籤的噬菌體庫。
噬菌體庫裡面含有適合不同應用的標籤,史密斯教授利用噬菌體庫的特性開發親和力篩選(affinity selection),如同抗體和抗原之間的專一性親和力。史密斯教授把目標抗原固定在基材上,與噬菌體庫混合,透過親和力篩選,僅有與目標抗原具強親和力的噬菌體能緊緊握住,其他會被洗掉,重複幾次就可得到與目標抗原具強親和力的胜肽標籤。
溫特開發抗體藥物
2018年諾貝爾化學獎得主溫特(Sir Gregory P. Winter)教授的研究興趣在免疫學,他一直想把人體B cell的抗體生成機制應用在抗體藥物開發中,千尋萬尋,發現噬菌體展示就是最好的工具。溫特教授把隨機突變方式製備出來抗體結合位(antibody binding site)的 DNA 片段植入噬菌體中,讓其表現在嗜菌體的表面,隨後利用親和力篩選方式進行多次篩選,找到親和力最強的抗體結合位。
溫特的技術廣泛應用於製備新藥上,2002年第一種利用「噬菌體展示」技術研發的新藥「Adalimumab」問世,用於治療風溼性關節炎、牛皮癬與腸道炎症。噬菌體展示也運用於研究腫瘤細胞、自體免疫疾病等。而目前在阿茲海默氏症的藥物研究上,也是利用噬菌體展示在噬菌體上製造許多抗體去結合蛋白質,找到最適合的抗體。
阿茲海默氏症是由一種特定的蛋白質與腦細胞的特定區域結合而誘發的疾病,利用噬菌體展示找到這個蛋白質最適合的抗體,讓抗體跟蛋白質結合,從而阻礙蛋白質與腦細胞的結合,期望能預防及減緩阿茲海默氏症的發病與惡化。目前已有超過60種進入臨床測試的抗體藥物是透過噬菌體展示開發出來。
阿諾德、史密斯和溫特教授們的研究創造了演化在應用化學領域的全新舞台,利用他們的技術及概念延伸,可擴及有利於環境、綠能源、藥物的研究,以解決空汙、能源危機、癌症等備受矚目的議題。或許將來某一天,藉由創新科學技術,水或酒精可完全取代汽油; 廢棄物可完全生物降解;癌症可藉由藥物預防及治癒。人類待解的課題很多,每一道題都有許多困難須克服。所幸,跟隨著科學家的腳步,與他們一同搭上小獵犬號——這樣的演化過程仍持續進行中。
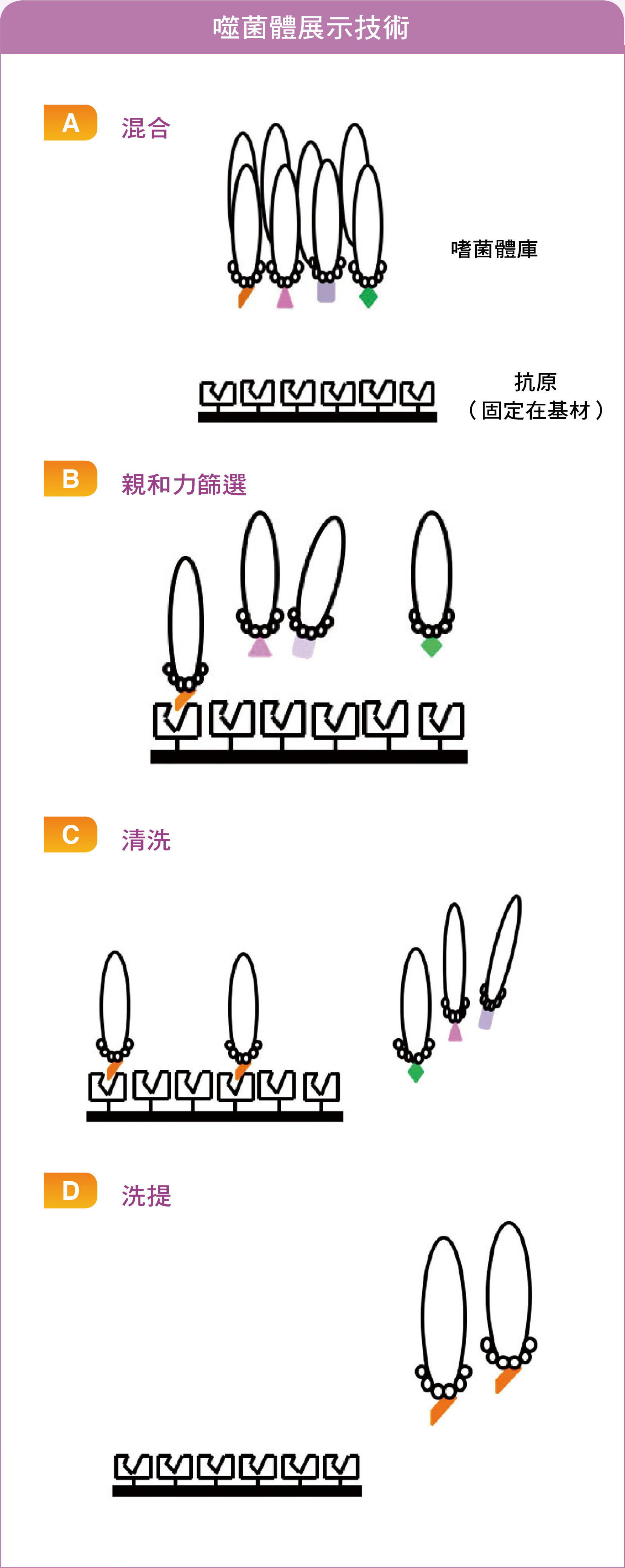 噬菌體展示技術:經過(A)~ (D)步驟後可得到對標的抗原具高度專一性的胜肽序列,若經過上述步驟所獲得的胜肽序列的專一性不如預期,可把(D)步驟所得到的噬菌體樣品重複進行(A)~ (D)步驟。
噬菌體展示技術:經過(A)~ (D)步驟後可得到對標的抗原具高度專一性的胜肽序列,若經過上述步驟所獲得的胜肽序列的專一性不如預期,可把(D)步驟所得到的噬菌體樣品重複進行(A)~ (D)步驟。
—————————————————————————————————————————————
註1:2018年諾貝爾化學獎得獎人為阿諾德(Frances H. Arnold)教授、史密斯(George P. Smith)教授及溫特(Sir Gregory P. Winter)教授,他們分別在蛋白質定向演化研究有著改變世界的傑出貢獻。
註2:2018年諾貝爾化學獎得獎人之一的阿諾德教授於1985年從加州大學柏克萊分校化學工程學系取得博士學位,她於攻讀博士學位期間,研究管柱分離(層析法)的理論,並藉由理論的幫助預測分子層析的行為。博士畢業後正值基因工程開始起飛的90年代,阿諾德教授於博士後研究的期間,開始了DNA的研究,並發表了一篇關於DNA配對錯誤行為的論文。
在DNA雙股螺旋結構中,鹼基A會和鹼基T配對,而鹼基G會和鹼基C配對,錯誤的配對則是突變的開始(配對錯誤雖會發生,但人體可是有修復機制的!)。若能了解配對錯誤的機制,則更能了解演化背後運行的原則。令人洩氣的是,在一篇論文中,她指出實驗數據還無法從化學鍵結角度回答鹼基錯誤配對的問題,這個結論也間接指出科學家要正確描述鹼錯誤配對的行為還很遠。
註3:酵素是催化劑,酵素與其他金屬催化劑不同的地方在於酵素分子是軟且具有彈性結構的物質。如果說酵素反應的反應物是鑰匙,酵素只有在正確的環境條件下才會摺疊成正確的鎖頭,鎖頭的正確性造就酵素的活性,影響反應的進行。酵素經長時間演化成適合在水相中進行反應,水分子與酵素分子所產生的氫鍵是雕塑酵素結構的重要弱作用力,這也展現水對生物的重要性是長期演化的結果。
若把枯草桿菌蛋白酶從水相放進有機相,溶劑分子勢必改變枯草桿菌蛋白酶原有的構形,而不利酵素催化功能。若能適當地改變枯草桿菌蛋白酶的胺基酸組成,勢必也能讓枯草桿菌蛋白酶在有機溶劑環境下形成可進行催化反應的構形。換言之,只要改變部分的枯草桿菌蛋白酶序列,就有辦法達到這樣的目標。
註4:隨機突變是以polymerase chain reaction(PCR)作為體外合成DNA片段的技術,藉由改變PCR的反應條件就能提高DNA合成的出錯率。由於DNA合成出錯於PCR過程是隨機的,因此當反應結束後,就能創造出錯誤配對的DNA片段資料庫,這個技術就稱為error-prone PCR。
註5:常用來作為噬菌體展示的噬菌體是f1、fd及M13,這幾種噬菌體都以大腸桿菌為宿主,DNA序列有高達98.5%的相似性,由於在顯微鏡下呈纖維狀(6 × 1000 nm),常稱為纖維型噬菌體。
 2018年諾貝爾化學獎得獎人阿諾德、史密斯和溫特教授們的研究創造了演化在應用化學領域的全新舞台,利用他們的技術及概念延伸,可擴及有利於環境、綠能源、藥物的研究,以解決空汙、能源危機、癌症等備受矚目的議題。
2018年諾貝爾化學獎得獎人阿諾德、史密斯和溫特教授們的研究創造了演化在應用化學領域的全新舞台,利用他們的技術及概念延伸,可擴及有利於環境、綠能源、藥物的研究,以解決空汙、能源危機、癌症等備受矚目的議題。 (上)生物在地球的演化史。紫色:前寒武紀出現的生物共同祖先藍綠菌,末期遇到一次環境改變;紅色:寒武紀大爆發,現今生物的各大類別突然出現,末期環境巨大變動;綠色:進入中生代,恐龍大量出現,但後期遇到星體撞地球,溫度變化使得冷血動物接連死亡;藍色:進入新生代,鳥類哺乳類昆蟲時代,後期開始有人類出現。(下) 定向演化示意圖,演化時間尺度是數天之譜。
(上)生物在地球的演化史。紫色:前寒武紀出現的生物共同祖先藍綠菌,末期遇到一次環境改變;紅色:寒武紀大爆發,現今生物的各大類別突然出現,末期環境巨大變動;綠色:進入中生代,恐龍大量出現,但後期遇到星體撞地球,溫度變化使得冷血動物接連死亡;藍色:進入新生代,鳥類哺乳類昆蟲時代,後期開始有人類出現。(下) 定向演化示意圖,演化時間尺度是數天之譜。 基因工程技術:利用基因工程技術把隨機突變所得到的胜肽庫嵌入噬菌體基因組得到噬菌體基因庫,進而得到表面帶有不同標籤的噬菌體庫。
基因工程技術:利用基因工程技術把隨機突變所得到的胜肽庫嵌入噬菌體基因組得到噬菌體基因庫,進而得到表面帶有不同標籤的噬菌體庫。 噬菌體展示技術:經過(A)~ (D)步驟後可得到對標的抗原具高度專一性的胜肽序列,若經過上述步驟所獲得的胜肽序列的專一性不如預期,可把(D)步驟所得到的噬菌體樣品重複進行(A)~ (D)步驟。
噬菌體展示技術:經過(A)~ (D)步驟後可得到對標的抗原具高度專一性的胜肽序列,若經過上述步驟所獲得的胜肽序列的專一性不如預期,可把(D)步驟所得到的噬菌體樣品重複進行(A)~ (D)步驟。