人類能夠返老還童嗎?科技能夠讓時光倒轉回到過去嗎?隨著胚胎的發育到長大成人,生老病死對人類像是不可逆的旅程。但近幾年的幹細胞研究突破,讓科學家看到生命逆轉的可能。
撥動生命時鐘的科學家
科學家過去總是認為,當生物體的幹細胞分化成為數百種身體細胞之後,就無法變回具有分化能力的幹細胞,細胞分化就如同生命流逝般的「不可逆」。但英國劍橋大學教授約翰.戈登(John Gurdon)與日本京都大學教授山中伸彌(Shinya Yamanaka)兩位2012年諾貝爾生理醫學獎得主,讓世人體認到自己對幹細胞研究的貧乏想像,石破天驚地敲開再生醫學大門。
 約翰.戈登(右3著紅色外套)(圖/Deryck Chan提供,Wikipedia)
約翰.戈登(右3著紅色外套)(圖/Deryck Chan提供,Wikipedia)
1962年在牛津大學動物系任教的約翰.戈登,透過開創性研究剔除青蛙卵的細胞核,再把青蛙小腸上皮細胞的細胞核注入無核的青蛙卵,取代原本的卵細胞核,成功孕育出完整且活生生的蝌蚪,順利長成青蛙,成為歷史上第一隻複製動物,證明即使是已分化完成的體細胞,依舊擁有完整的基因資訊。
小腸上皮細胞是幹細胞分化後的體細胞,成為青蛙身體的一部分,就失去分化能力;但戈登卻重新找回它再發育的潛能,把體細胞核轉移到無核的卵、孕育變成蝌蚪,再長成青蛙。1996年轟動世界的桃莉羊,也是應用戈登的體細胞核轉移技術,成功培育的第1隻哺乳類複製動物,再次印證體細胞具備完整的基因資訊。
以iPod為期許——山中伸彌的iPS細胞
也許是今生註定的巧合,1962年出生的山中伸彌,在41年後受到體細胞核轉移技術的啟發,認為體細胞既然可以和卵結合變成完整的個體,應該也有變回幹細胞的可能。2006年他成功發明把體細胞「還原」成幹細胞的技術,找到4個關鍵基因,導入小鼠的皮膚纖維母細胞,變回具有分化功能的幹細胞。這種產製幹細胞的方法被學界稱為細胞「重新編程」,由體細胞誘導而成的人工幹細胞,則被命名為誘導性多能幹細胞(Induced pluripotent stem cell),也就是鼎鼎大名的「iPS細胞」。
但誘導性多能幹細胞的是英文簡寫,為甚麼不是大寫的「IPS」細胞,而是特別用小寫的「i」呢?這其實是山中伸彌本人的巧思,蘋果公司推出數位音樂播放器iPod,在2006年風靡全球,他希望誘導性多能幹細胞能夠跟iPod同樣受到世人的喜愛,因而將其命名為iPS細胞。也如同他的期許,iPS細胞很快在全世界颳起旋風,並持續至今。
如何找出細胞的變身關鍵?
雖然生命個體的基因資訊幾乎相同,但不同的基因表現,就會讓體內的細胞呈現不同的樣貌。山中伸彌從胚胎幹細胞與成熟體細胞基因表現不同之處著手,嘗試尋找讓體細胞「還原」成幹細胞的鑰匙,比較兩者差異後,找到24個很特別、僅在胚胎幹細胞才會發揮功用的基因(即轉錄因子);更神奇的是,當他將這些基因植入小鼠的皮膚纖維母細胞,竟然讓皮膚纖維母細胞外表變得與幹細胞極為相似,甚至出現細胞增生的特徵。
為了尋找不可或缺的關鍵基因,山中伸彌藉由逐一刪去法測試這24個基因,找出哪些基因會影響細胞轉換,最後篩選出4個關鍵性轉錄因子:Oct4、Sox2、Klf4、c-Myc,簡稱OSKM,並稱呼他們為「山中因子」(Yamanaka Factors)。藉著「山中因子」,iPS細胞不僅擺脫「幹細胞必須來自胚胎」的傳統觀念,也避開破壞胚胎的倫理道德爭議。
擺脫早期幹細胞研究的沉重枷鎖
1996年桃莉羊誕生,讓「幹細胞」真正印刻在大眾的視野。即使如此,科學家還是必須透過卵細胞及體細胞核的結合,從人工培育的胚胎取得幹細胞,「形成胚胎」似乎成為不可忽略的流程。若將此技術應用至人類,依舊會衍生出眾多爭議,例如卵細胞從哪裡來?是否會助長人類卵細胞非法買賣?細胞核轉移過程安全嗎?用人工受精卵培育的胚胎算是生命嗎?利用胚胎治療,算不算以命換命?會不會因此出現複製人?
 現存於蘇格蘭國立博物館的桃莉羊標本。(圖/Sgerbic提供,Wikipedia)
現存於蘇格蘭國立博物館的桃莉羊標本。(圖/Sgerbic提供,Wikipedia)
諸多倫理及道德的難題,讓人類胚胎幹細胞研究難以進一步發展。山中伸彌的iPS細胞完美避開所有爭議,不但不必使用卵細胞,更不需要胚胎就能夠培育出具有分化功能的幹細胞。
iPS細胞的風險與展望
雖然iPS細胞是劃時代的新技術,仍有諸多疑慮需要個個破解。首先,細胞是肉眼看不見的微小單位,被喻為「生命的積木」,要如何把這四個「山中因子」精準且成功送入小小的細胞,就是不簡單的學問。山中伸彌利用病毒當運送工具,把基因嵌入皮膚纖維母細胞DNA,學界統稱這些運送工具為「載體」。在山中伸彌之後,不斷有科學家發展出各式各樣的載體運送「山中因子」,像是聚合物和微脂體等,而不同的載體、不同的導入方式,都會影響培育iPS細胞的效率與安全性。
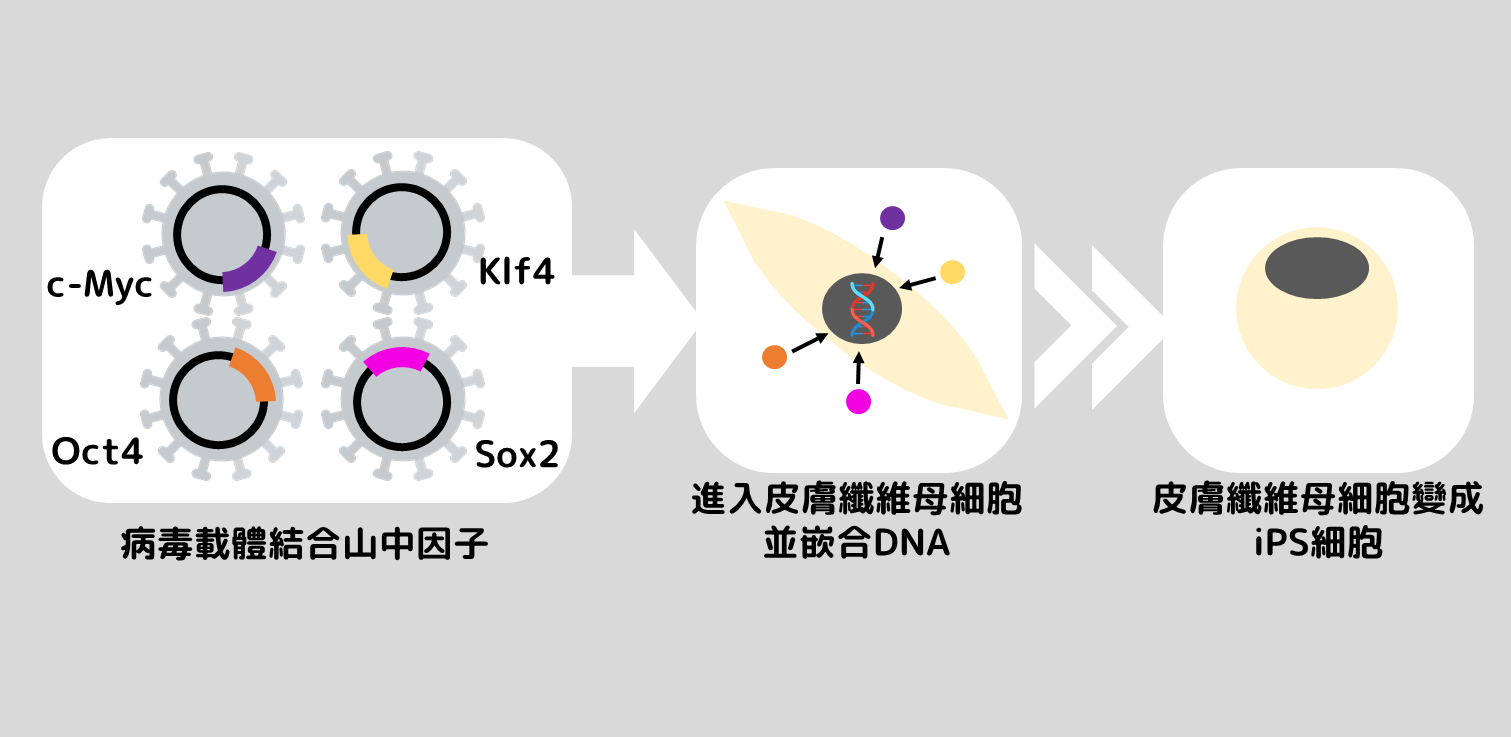 以病毒為載體將山中因子嵌入皮膚纖維母細胞製作成iPS細胞示意圖。(圖/陳儀珈繪製)
以病毒為載體將山中因子嵌入皮膚纖維母細胞製作成iPS細胞示意圖。(圖/陳儀珈繪製)
以病毒作為載體最大優點是成功機率高,可以順利地將「山中因子」嵌入體細胞DNA;然而病毒像是挑剔的小麻煩精,總是偏好把基因嵌入DNA特定位置,很容易影響原本體細胞基因表現,引發麻煩的副作用。與病毒相比,改用聚合物(許多小分子連結而成的巨大分子)或微脂體(磷脂質構成的微型空心球)當載體,雖然安全疑慮相對較低,但成功率較差。不同載體各有優缺點,目前仍有魚與熊掌難兼得的困擾。
除了載體選擇可能有安全風險,四個山中因子中的c-Myc,被醫界認為是致癌風險基因,可能與癌細胞的滋生有關,也成為iPS細胞治療的安全顧慮。不過就如同病毒以外的載體陸續應運而生,科學家也積極致力尋找c-Myc替代物質,改善iPS細胞造成的癌化風險,未來發展仍然精彩可期。
儘管iPS細胞技術未臻完美,除了載體與致癌基因外,基礎研究與臨床應用仍有諸多瓶頸,需要更多科學家參與才能突破。大家在驚嘆科學卓越研究成果的同時,更要審慎思考與評估,探尋新興科技背後潛在的危機,找到人類健康與科研發展共榮之道。
本著作係採用 創用 CC 姓名標示─非商業性─禁止改作 3.0 台灣 授權條款 授權.
本授權條款允許使用者重製、散布、傳輸著作,但不得為商業目的之使用,亦不得修改該著作。 使用時必須按照著作人指定的方式表彰其姓名。
閱讀授權標章或
授權條款法律文字。